COVID-19
Ultimo aggiornamento: giugno 2022. La pagina verrà aggiornata due volte all'anno
It looks like you are using an older version of Internet Explorer which is not supported. We advise that you update your browser to the latest version of Microsoft Edge, or consider using other browsers such as Chrome, Firefox or Safari.
Ultimo aggiornamento: giugno 2022. La pagina verrà aggiornata due volte all'anno
Novartis monitora regolarmente i casi di Covid-19 nei pazienti trattati con fingolimod. Basato sulla totalità dei dati disponibili dalle segnalazioni di casi COVID-19 nel contesto post-marketing e dall'analisi completa dei dati della MS Data Alliance Global Data sharing initiative1
Contesto post-marketing

Nei 9 casi di sperimentazione clinica
aQuesta sezione fornisce una sintesi dei casi di pazienti trattati con fingolimod che si sospetta abbiano contratto, o in cui è stato segnalato, COVID-19 come riportato nel database di sicurezza di Novartis, incluse le segnalazioni spontanee inviate volontariamente e i casi identificati nella letteratura scientifica. In genere, in questo contesto è presente una sottosegnalazione e, per tale motivo, il vero numeratore è sconosciuto. Anche il denominatore non è noto in quanto il numero effettivo di pazienti trattati con fingolimod non è prontamente disponibile. Molti dei casi contengono informazioni molto limitate e includono casi persi al follow-up. Pertanto, a causa di tali limitazioni, non è possibile trarre conclusioni rilevanti riguardo all’incidenza di COVID-19 o al decorso della malattia in pazienti che ricevono fingolimod.
Casi confermati di infezione da COVID-192,3
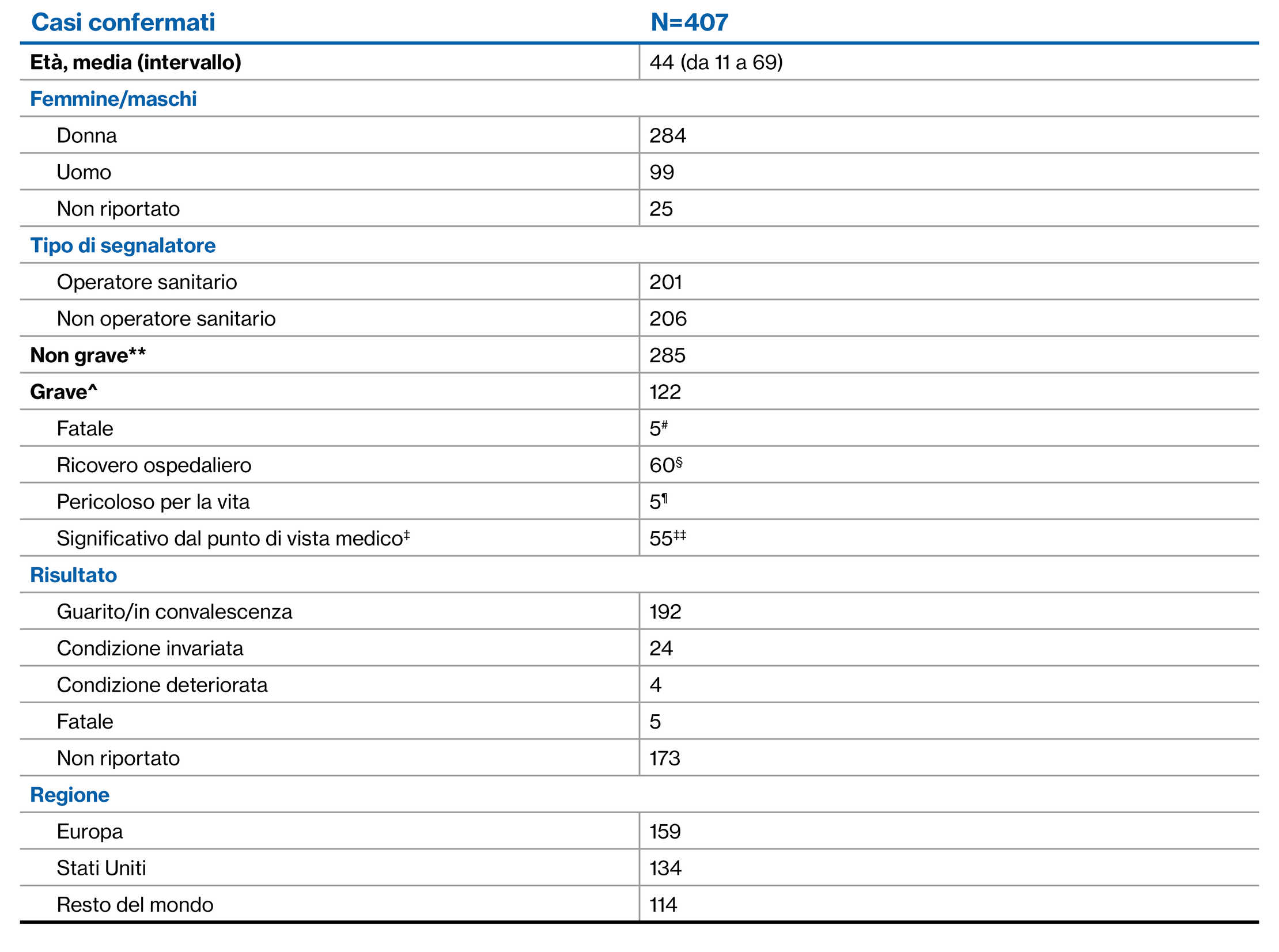
Risposta clinica alla vaccinazione anti-COVID-19
Impatto del COVID-19 nella SM in un contesto di real-world

This website is for non-promotional purposes and is intended for providing
safety information for healthcare professionals (HCP) only
Please confirm that you are an HCP
For HCPs: Information on this website is not country specific, and may contain information that is outside the approved indications in the country in which you are located. Please contact your local Novartis representative for the latest information specific to your country.
For non-HCPs / patients: This safety website is available for HCPs only