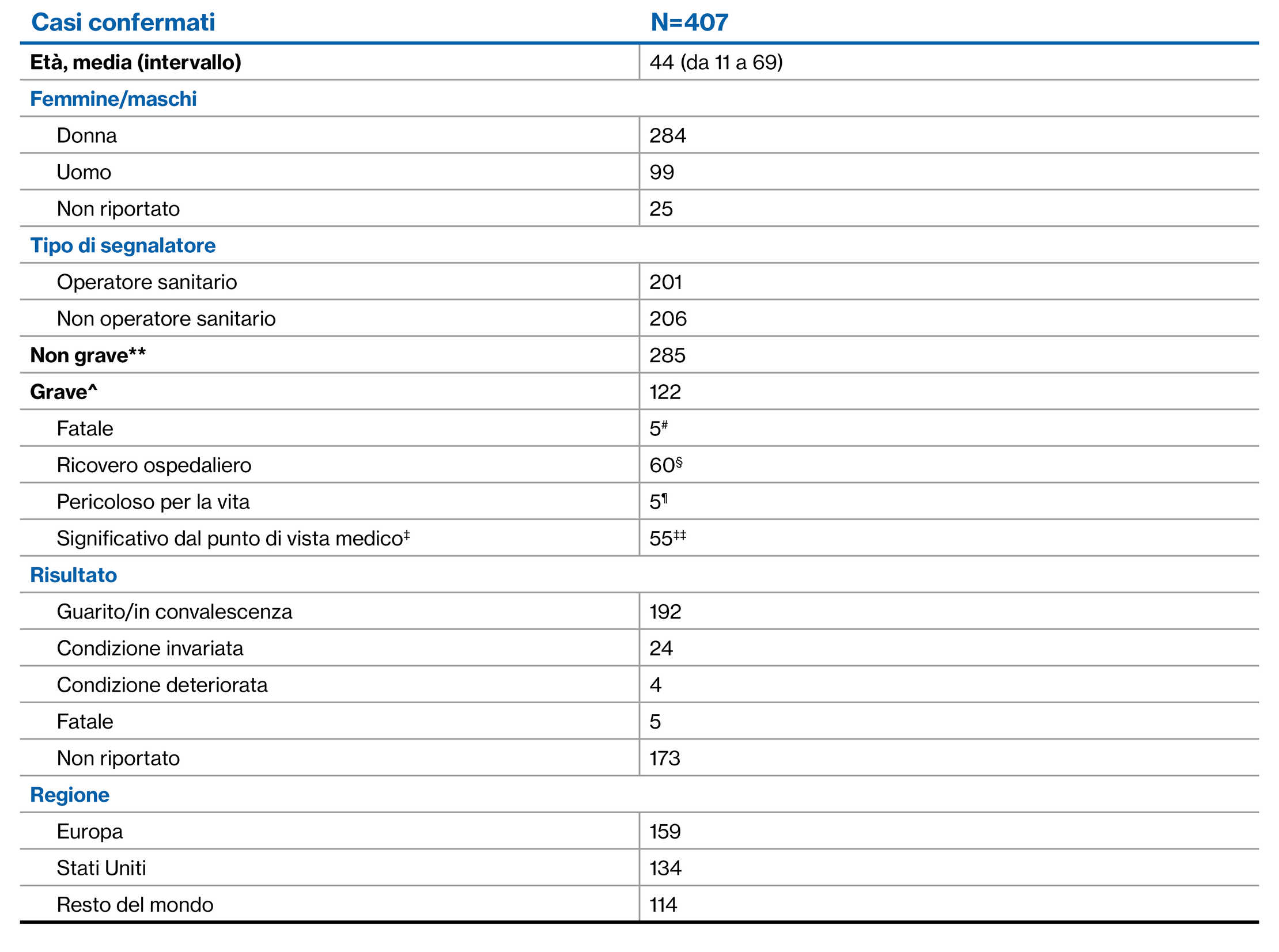
Casi confermati di infezione da COVID-192
**riferito come non grave
^Accertato in base ai criteri più gravi.
#Un paziente (età 66 anni) presentava molteplici fattori di rischio (dettagli non riportati); un paziente (età 39 anni) presentava SM secondariamente progressiva attiva; un paziente (età 45 anni) presentava disturbo misto del tessuto connettivo non specificato; un paziente aveva 64 anni di età e non disponeva di dettagli relativi all’anamnesi medica; un paziente (età 42 anni) ha sviluppato un’infezione batterica disseminata e shock settico.
§13 casi su 17 (in cui sono state riportate informazioni) con uno o più fattori di rischio di COVID-19. Sono stati osservati anche due pazienti con esito fatale ricoverati in ospedale e un caso segnalato come potenzialmente letale è stato segnalato come ricoverato in ospedale.
¶2 casi sono stati segnalati da non HCP, tra cui un paziente senza ulteriori dettagli forniti e un altro paziente con malattia lieve.
‡Evento medico importante che potrebbe non essere immediatamente potenzialmente letale o comportare il decesso o il ricovero, ma potrebbe mettere a rischio il paziente o richiedere un intervento per prevenire uno degli altri esiti gravi.
‡‡La maggioranza, 39 casi, è stata ricevuta da non HCP.
Gravità ed esito del COVID-192
NOTA: La gravità dei casi è stata valutata in base alle scale di gravità del COVID-19 dell’Ente statunitense preposto al controllo di alimenti e farmaci (Food and Drug Administration)3 e dell’Organizzazione mondiale della sanità4 da parte di un comitato di valutazione indipendente comprendente esperti in SM e malattie infettive e laddove erano disponibili dati, la categorizzazione è stata effettuata come segue: asintomatica (infezione senza sintomi), lieve (che non richiede il ricovero, non includeva dispnea), moderata (ricovero ospedaliero con polmonite non segnalata come grave e/o con frequenza respiratoria [Respiratory Rate, RR] >20 e/o saturazione d’ossigeno [SpO2] >90%, respiro affannoso o dispnea, ricoveri in ospedale inferiori a 7 giorni senza ulteriori dettagli); grave (polmonite segnalata come grave – RR ≥30, SpO2 ≤93%, ricovero in ospedale 7 giorni o più senza ulteriori dettagli), o critica (insufficienza respiratoria e/o intubazione).
I numeri tra parentesi indicano – (pazienti ricoverati; pazienti che necessitano di ventilazione, CPAP o ricovero in UTI)
+Outcome is not application as these patients are asymptomatic.
ǁNon tutti i casi moderati sono stati ricoverati.
ǂUn paziente (età 66 anni) presentava molteplici fattori di rischio (dettagli non riportati); un paziente (età 39 anni) presentava SM secondariamente progressiva attiva; un paziente (età 45 anni) presentava disturbi misti non specificati del tessuto connettivo; un paziente aveva 64 anni di età senza fornire dettagli relativi all’anamnesi medica; un paziente (età 42 anni) sviluppava un’infezione batterica disseminata e shock settico.
Questa sezione fornisce una sintesi dei casi di pazienti trattati con fingolimod che si sospetta abbiano contratto, o in cui è stato segnalato, COVID-19 come riportato nel database di sicurezza di Novartis, comprese le segnalazioni spontanee inviate volontariamente e i casi identificati nella letteratura scientifica. In genere, in questo contesto è presente una sottosegnalazione, pertanto il vero numeratore è sconosciuto. Anche il denominatore non è noto, poiché il numero effettivo di pazienti in terapia con fingolimod non è prontamente disponibile. Molti dei casi contengono informazioni molto limitate e includono casi persi al follow-up. Pertanto, a causa di queste limitazioni, non è possibile trarre conclusioni significative sull’incidenza di COVID-19 o sul decorso della malattia nei pazienti che ricevono fingolimod.
Impatto del COVID-19 nella SM in un contesto di real-world
- La SM è una patologia neurodegenerativa infiammatoria cronica autoimmune del SNC in cui i pazienti sono generalmente trattati con immunosoppressori o immunomodulatori.5 L’attuale pandemia di COVID-19 ha destato preoccupazioni in merito alla risposta immunitaria alle infezioni virali nei pazienti con SM trattati con terapie modificanti la malattia6
- La condivisione e le analisi complete dei dati riguardanti l’effetto del COVID-19 nelle persone affette da SM sono state condotte da: COVID-19 nella SM - GDSI.9L’iniziativa GDSI è un’iniziativa congiunta della Federazione internazionale della SM (MS International Federation) e di MS Data Alliance, che opera sotto l’egida della Fondazione europea Charcot (European Charcot Foundation) e in collaborazione con molti partner (di dati) in tutto il mondo
- Nelle persone affette da SM, l’incidenza di COVID-19 varia dallo 0,5% all’1,13%.7 È stato riportato che la mortalità dovuta a COVID-19 va dal 3,25% al 4,2%1,7,8
- Secondo la MS International Federation,le evidenze disponibili indicano che le persone affette da SM che assumono fingolimod non presentano un rischio maggiore di sintomi più gravi di COVID-199