FREEDOMS
Conception de l’étude
Étude de phase 3 de deux ans, en double aveugle, randomisée, contrôlée par placebo, chez des adultes atteints de SEP-RR
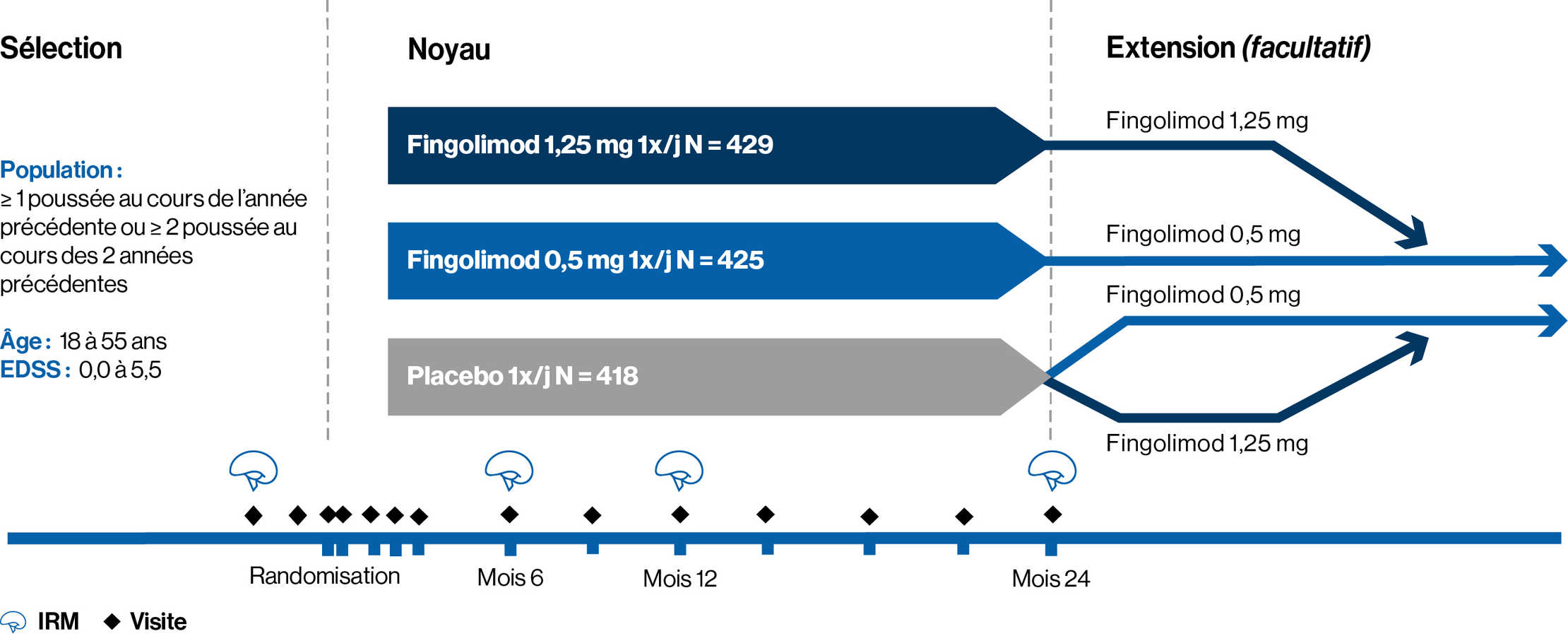
Une étude de phase 3 de deux ans, randomisée, en double aveugle, contrôlée par placebo, menée chez 1 272 adultes atteints de SEP-RR
Les patients ont été randomisés pour recevoir une dose quotidienne unique de fingolimod 0,5 mg (n = 425) ou 1,25 mg (n = 429) ou un placebo correspondant une fois par jour (n = 418) pendant 2 ans
Caractéristiques des patients à l’inclusion :
1. Âgé entre 18 et 55 ans
2. Un diagnostic de SEP-RR avec au moins 1 poussée documentée au cours de l’année précédente ou au moins 2 poussées documentées au cours des 2 années précédentes
3. Un score de 0,0 à 5,5 sur l’échelle EDSS. Le score médian à l’inclusion était de 2,0
Critère d’évaluation principal : TAP
Critère d’évaluation secondaire clé : délai jusqu’à la progression confirmée du handicap à 3 mois, telle que mesurée par une augmentation du score EDSS d’au moins 1 point par rapport à l’inclusion (augmentation de 0,5 point pour les patients dont le score EDSS à l’inclusion était de 5,5) maintenue pendant 3 mois*
Les critères d’évaluation secondaires supplémentaires comprenaient le nombre de lésions Gd+ en T1 et le nombre de lésions nouvelles ou nouvellement élargies sur les IRM pondérées en T2
* L’analyse d’un critère d’évaluation secondaire clé comprend la même population en intention de traiter que le ou les critères d’évaluation principaux, ainsi que la régression logistique ajustée pour certaines caractéristiques de l’échantillon à l’inclusion
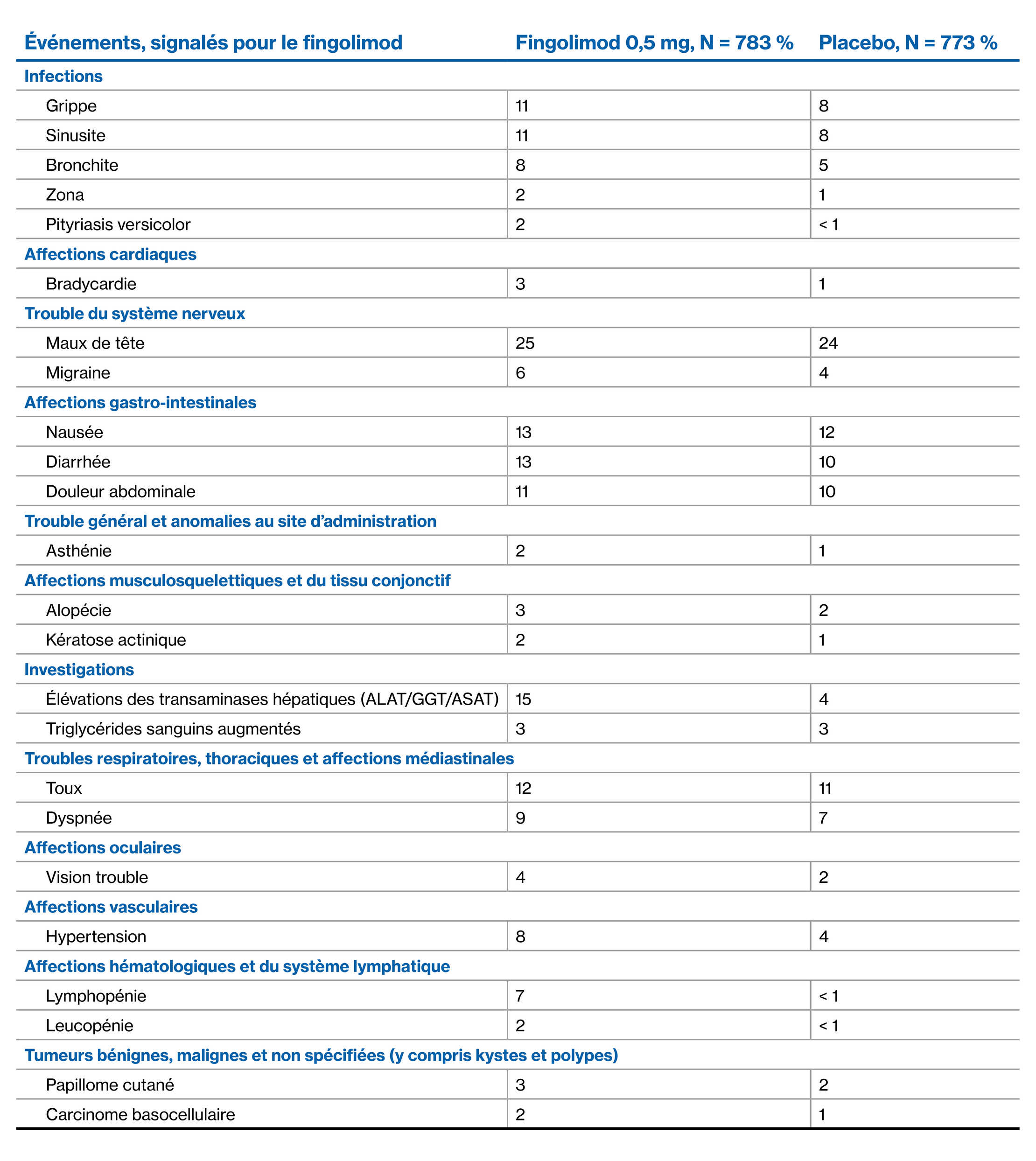
Profil d’EI du fingolimod par rapport au placebo sur 2 ans : Études FREEDOMS et FREEDOMS II1
Profil d’EI du fingolimod sur 4 ans : Étude d’extension FREEDOMS2