ASSESS
Conception de l’étude
Étude de phase 3b d’un an, randomisée, contrôlée contre substance active, à dose et évaluateur en aveugle, en groupes parallèles, menée chez des adultes atteints de SEP-RR
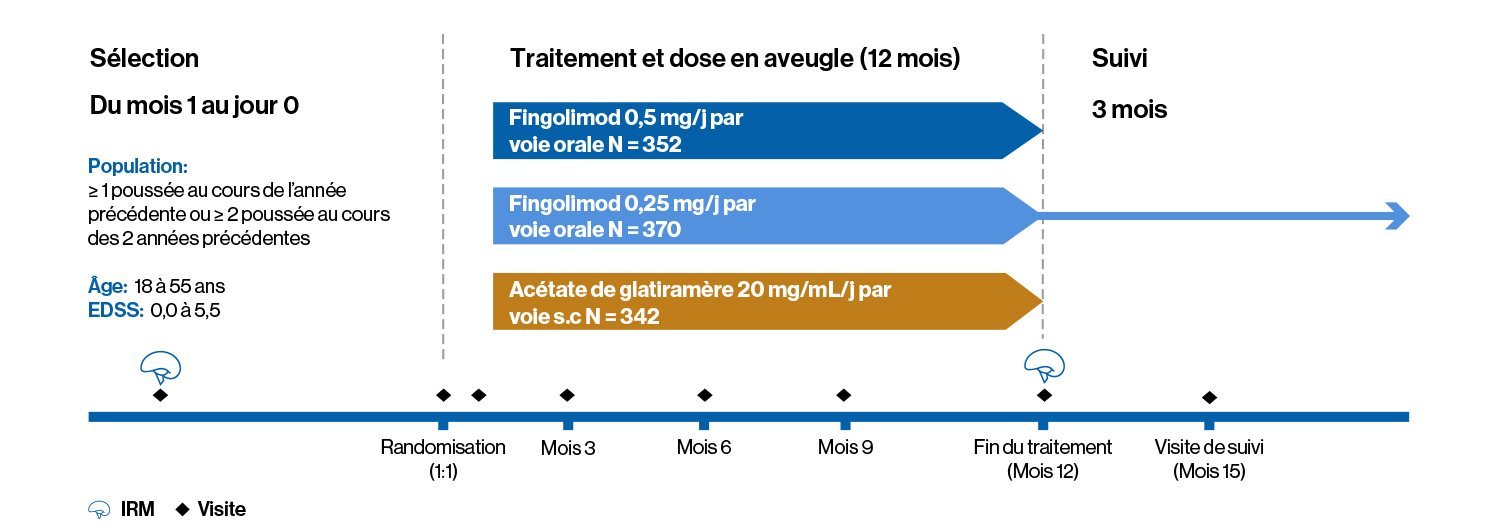
EDSS, échelle étendue du statut d’invalidité [Expanded Disability Status Scale] ; IRM, imagerie par résonance magnétique ; SEP-RR, sclérose en plaques récurrente-rémittente ; s.c., sous-cutané ; Bruce Cree, et al Efficacy and safety of Fingolimod 0.5 mg and 0.25 mg Versus Glatiramer Acetate 20mg in Patients with Relapsing-Remitting Multiple Scierosis - Groupe de l’étude ASSESS.
Neurology Apr 2019, 92 (15 Supplement)S56.009
Étude SQ de phase 3b, randomisée, en aveugle de la dose, en aveugle pour l’évaluateur, contrôlée contre substance active (injection d’acétate de glatiramère) menée sur 1 an, menée chez des adultes atteints de SEP-RR. Les patients ont été affectés de manière aléatoire pour recevoir du fingolimod 0,25 mg et 0,5 mg une fois par jour, par rapport à des injections sous-cutanées une fois par jour d’acétate de glatiramère 20 mg. À l’inclusion, les patients atteints de SEP-RR âgés de 18 à 65 ans (médiane 39 ans) présentaient ≥ 1 poussée documentée au cours de l’année précédente ou ≥ 2 poussées documentées au cours des 2 années précédentes, et avaient un score de 0,0 à 6,0 sur l’échelle EDSS (le score médian était de 2,5 à l’inclusion). Le critère d’évaluation principal était le TAP
Profil des EI du fingolimod par rapport à l’acétate de glatiramère : Étude ASSESS1