TRANSFORMS
研究设计
在 RRMS 成人中进行的双盲、随机、双模拟、活性药物对照、1 年 III 期研究
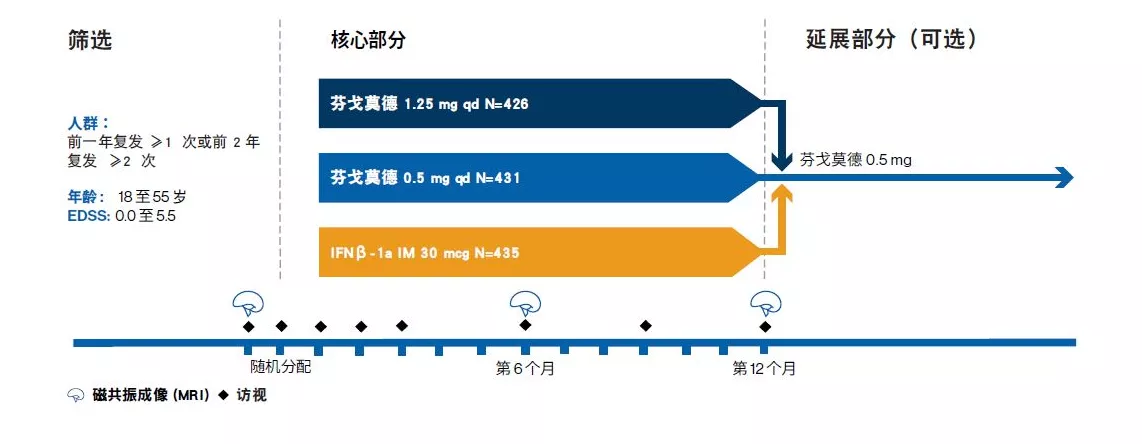
研究设计:
一项包含 1292 名 RRMS 成人的 1 年、随机、双盲、双模拟、活性药物对照 (IFNβ-1a IM) III 期研究
患者被随机分配接受芬戈莫德 0.5 mg (n=431) 或 1.25 mg (n=426) 每日一次或 IFNβ-1a IM 注射,每周剂量为 30 μg (n=435),持续 1 年
患者基线特征:
1. 18 至 55 岁
2. 诊断为 RRMS,在前一年有至少 1 次复发记录,或在前 2 年有至少 2 次复发记录
3. 扩展残疾状态量表 (EDSS) 评分为 0.0 至 5.5。基线时的中位评分为 2.0
4. 既往接受任何类型的干扰素-β 或醋酸格拉替雷治疗不属于排除标准
主要终点:主要目的是证明芬戈莫德 0.5 mg 在针对 RRMS 患者的长达 12 个月的治疗中在 ARR 方面优于 IFNβ-1a。两个关键次要终点:1 年时 T2 加权 MRI 扫描中新发或新增大的高信号病灶数量和到 3 个月确认残疾进展的时间,通过 EDSS 较基线至少增加 1 分来测定(基线 EDSS 为 5.5 的患者增加 0.5 分),持续 3 个月
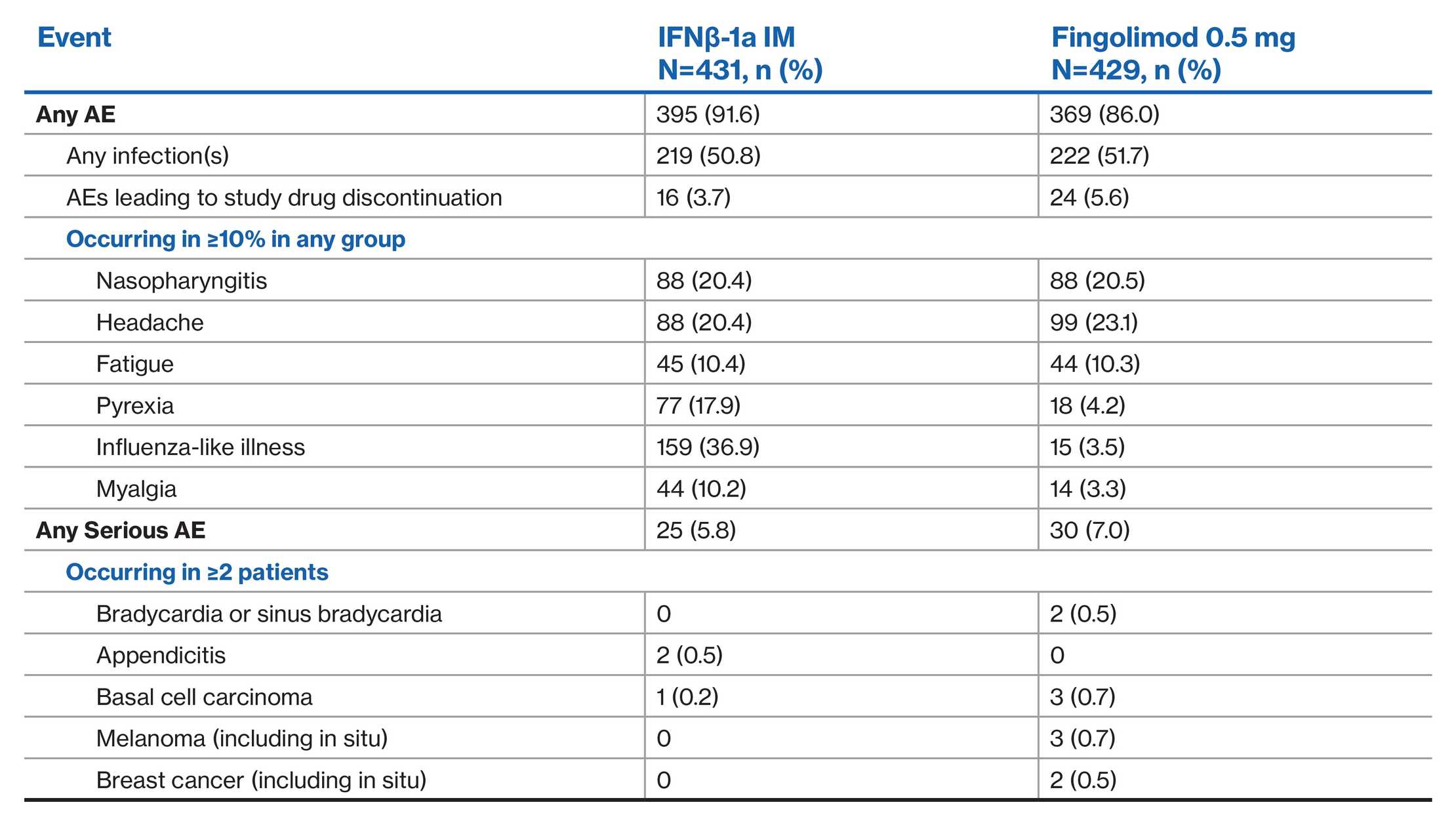
1 年内芬戈莫德对比干扰素的不良事件情况:TRANSFORMS 核心研究1
芬戈莫德在 4.5 年内的不良事件情况:TRANSFORMS 扩展研究2**
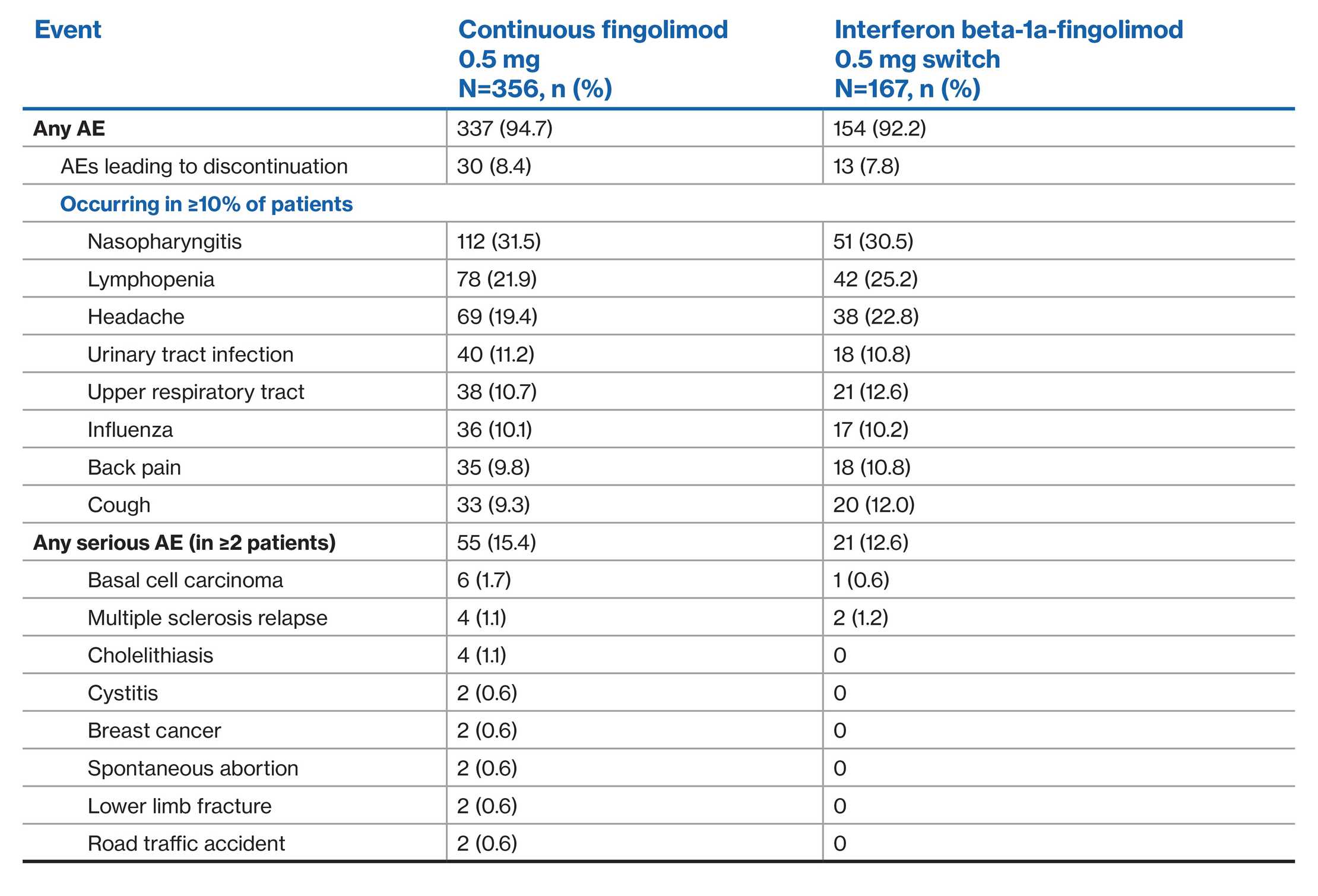
**所有患者均在扩展期接受芬戈莫德 0.5 mg
