PARADIGMS
研究设计
在 RRMS 儿童患者中比较干扰素 β-1a 的双盲、随机、活性药物对照两年研究**
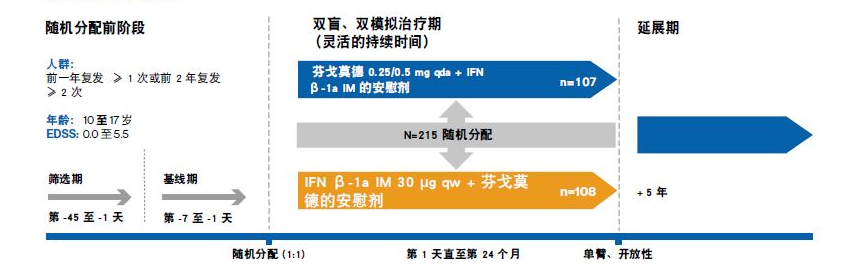
**芬戈莫德尚未在 10 岁以下儿童中进行过研究
一项双盲、随机、临床试验,旨在比较芬戈莫德 0.25 mg 或 0.5 mg(根据体重选择的剂量)每日一次与肌内 (IM) 干扰素 β-1a 30 mcg 治疗 215 例 10 岁至 18 岁以下儿童 RRMS 的疗效和安全性
患者基线特征:
1. RRMS 诊断基于经修订的儿童 MS 共识定义,其中包括 2010 年 McDonald 标准
2. EDSS评分:0-5.5。基线时的中位评分为 1.5
3. 既往经治或未经治疗的患者,在过去一年中至少有 1 次复发,或在过去 2 年内有 2 次复发,或至少 1 次 Gd+ 的证据
随机前 6 个月 MRI 提示有 T1 病灶
4. 无进展性 MS 或其他免疫系统疾病或其他脱髓鞘疾病、急性播散性脑脊髓炎、
或视神经炎的证据
主要终点:年化复发率,定义为活性治疗期间确认的每年复发的平均次数
关键次要终点:T2 加权 MRI 测得相较于基线的新发或新增大病灶的年化发生率
其他次要终点:
1. 对 Gd+ T1 病灶的影响
2. 安全性和耐受性
要求患者在接受第一剂研究药物后留在研究中心至少 6 小时(即第 1 天进行首次给药监测)。首次给药观察包括监测生命体征(心率和血压)、潜在心动过缓体征和心电图
允许既往使用干扰素-β、富马酸二甲酯或醋酸格拉替雷治疗,直至随机分组
筛选时进行基线评估和神经系统评估。每 3 个月和疑似复发时完成额外的神经系统评估筛选时进行 MRI 评估,且研究期间每 6 个月进行一次
**芬戈莫德尚未在 10 岁以下儿童中进行过研究
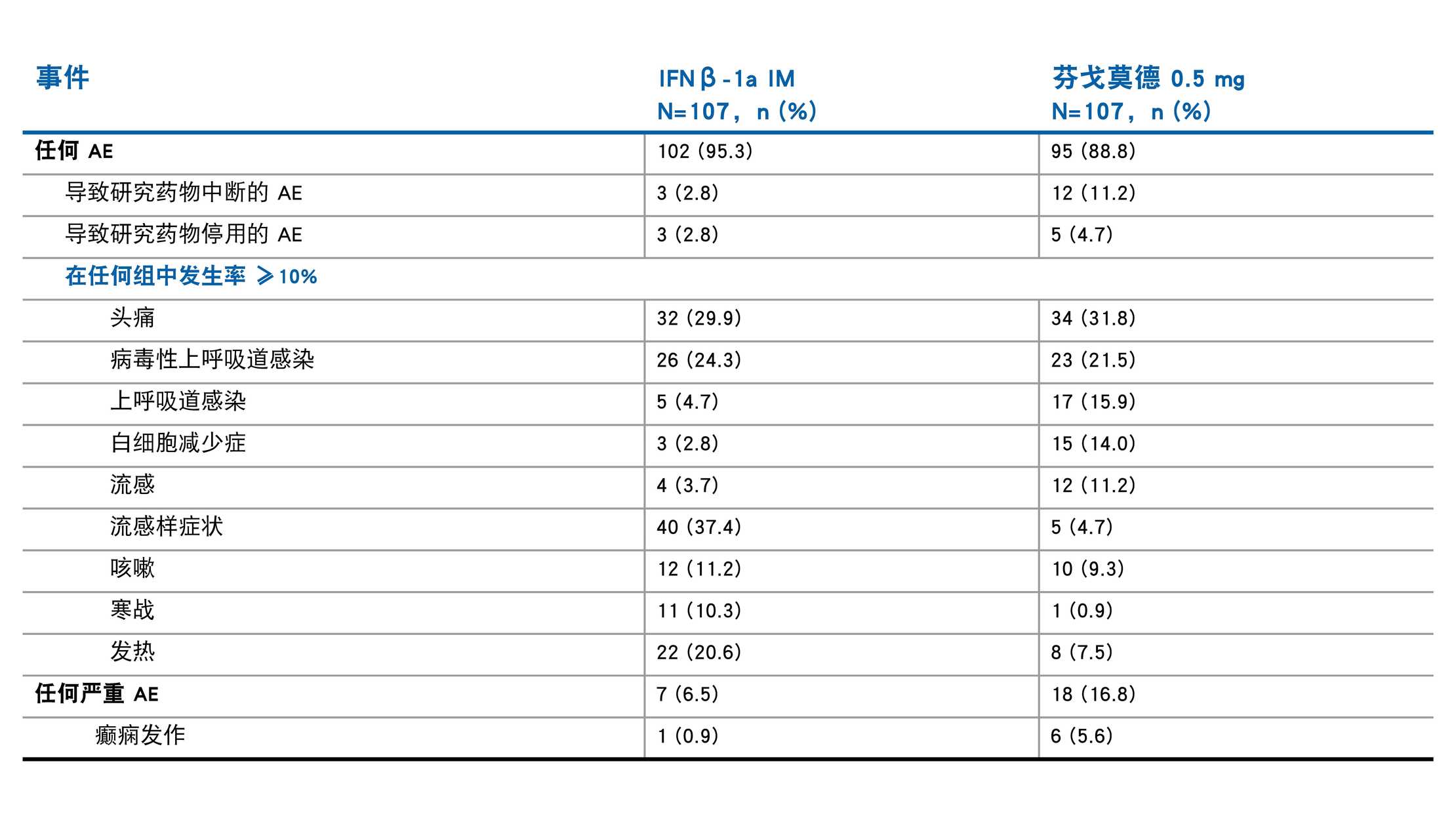
芬戈莫德对比干扰素的不良事件情况:PARADIGMS 双盲治疗期1
芬戈莫德在 4.7 年内的不良事件情况:PARADIGMS 扩展研究(中期分析)2
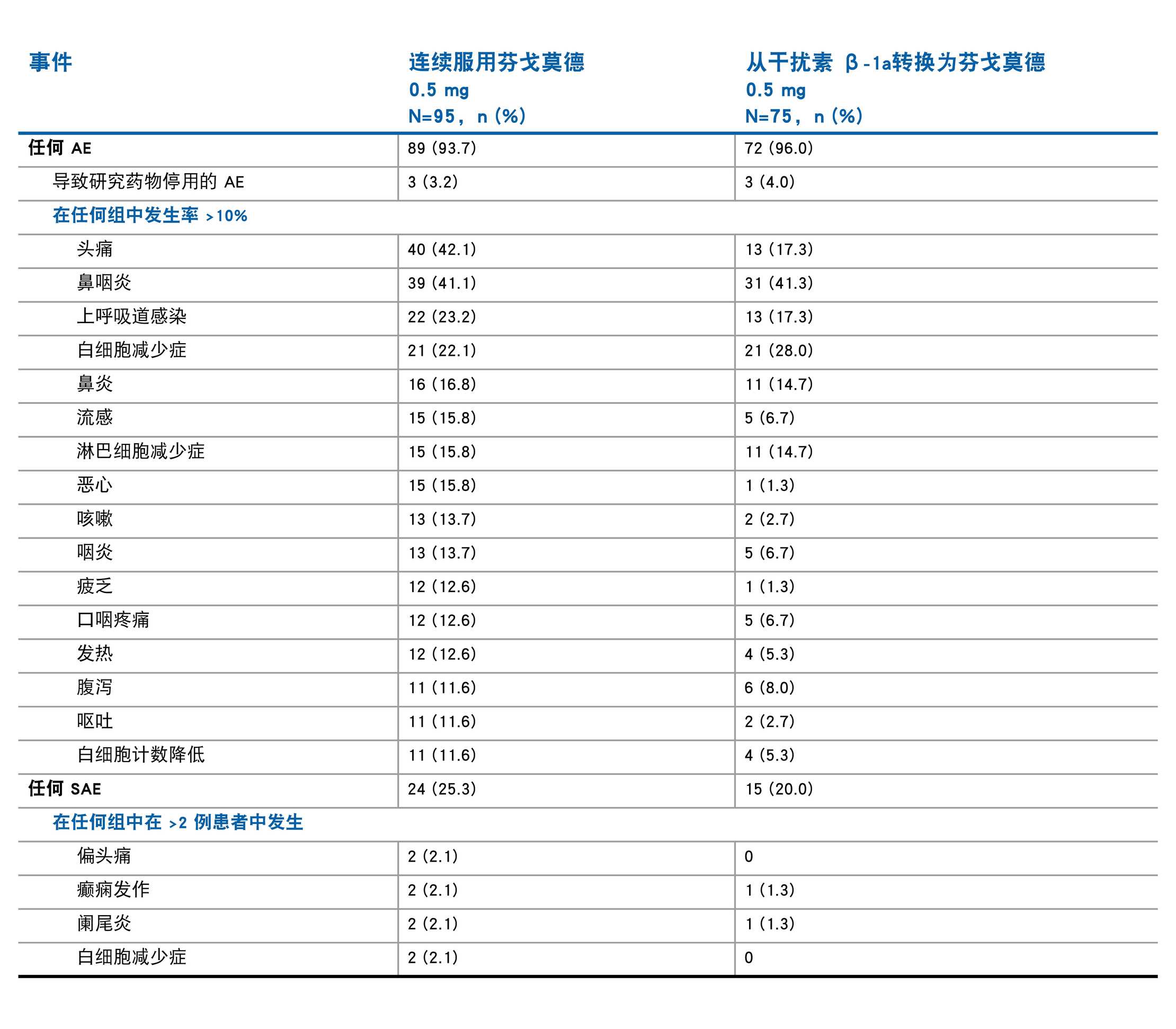
注意:由于本分析性质为中期分析,因此所显示的数据在最终数据库锁定前可能会发生变化。
