COVID-19
1Sullivan R 等著。芬戈莫德或西尼莫德治疗患者病例系列中的COVID-19 感染。
图:在芬戈莫德治疗的多发性硬化患者最后一次访视时的COVID-19严重程度* 和转归
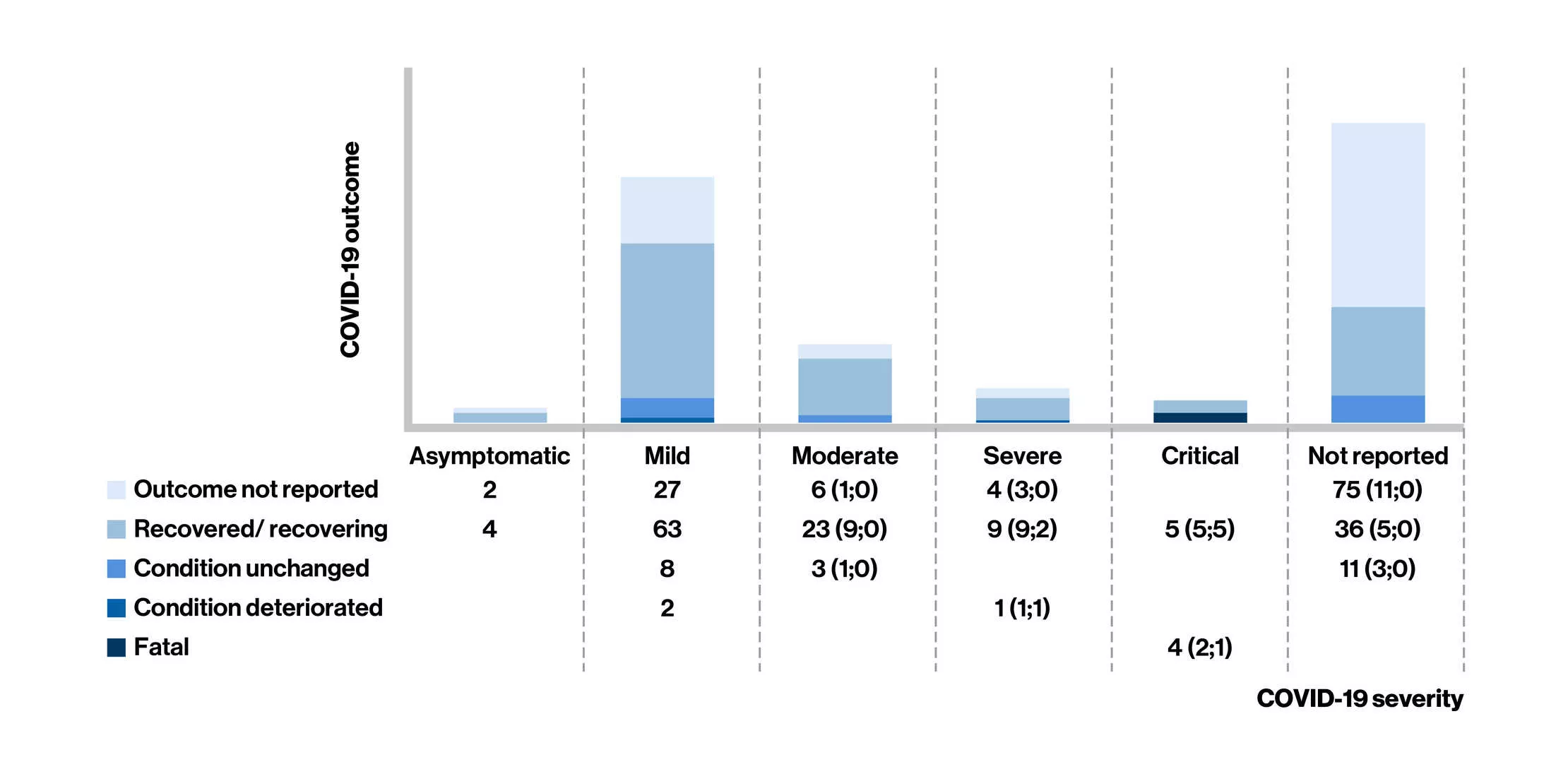
- 芬戈莫德治疗的 MS 患者[平均年龄:44 岁;女性 (73%)]报告了283例确诊COVID-19病例,其中161 名患者报告了病例严重程度(无症状,n = 6;轻度,n = 100‘中度,n = 32;50 例病例需要住院治疗)
图:西莫尼德治疗的多发性硬化患者在最后一次访视时COVID-19的严重程度* 和转归
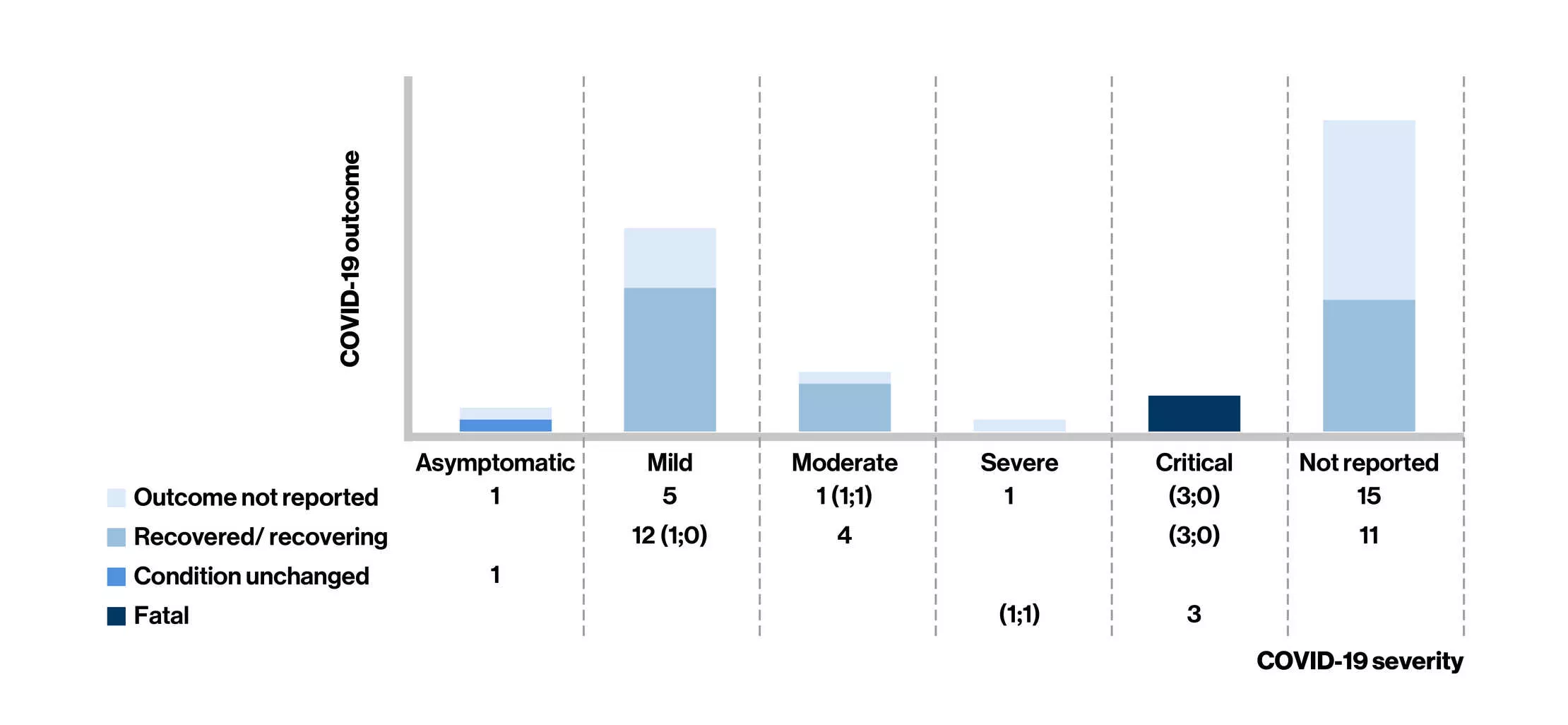
- 在西莫尼德治疗的MS 患者中[平均年龄:54 岁;女性 (68%)],有54 例 COVID-19 确诊病例中(45 例来自售后背景,9 例来自正在进行的开放标签临床试验),有28例报告了病例严重程度(无症状,n = 2;轻度,n = 17或中度,n = 5;9例需要住院治疗)
接受芬戈莫德治疗的患者出现更严重COVID-19症状的风险似乎与在患COVID-19的普通人群和 MS人群中报告的风险相似。对于西莫尼德,报告的病例数量较少,加上信息不足,排除了有意义的结论。
缩写
COVID-19,新型冠状病毒肺炎;MS,多发性硬化
新信息
实际循证
UCSF 纵向研究:中期分析
2Sabatino J 等著。使用抗CD20疗法和鞘氨醇-1-磷酸受体调节剂的多发性硬化症患者在额外接种SARS-CoV-2疫苗后的适应性免疫的纵向分析。
图:不同组在每个时间点对SARS-CoV-2疫苗接种的抗体反应
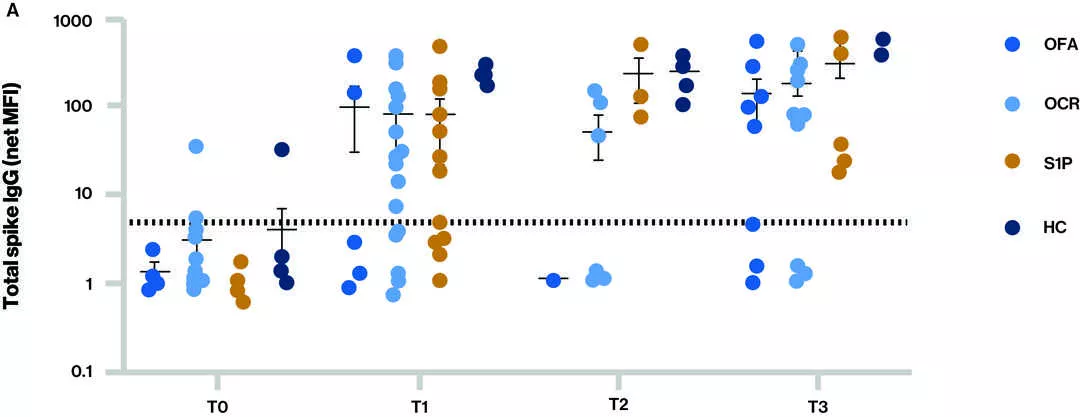

图A和B中的虚线表示血清阳性的截止值;血样采集的时间点(T):T0–基线,T1–接种两剂疫苗后采集的样本,T2–接种3剂疫苗(加强针)前采集的样本和T3–接种三剂疫苗(加强针)后采集的样品;S1P(芬戈莫德和西莫尼德)
- 在每个时间点,不同组的总Spike(A)和Spike RBD(受体结合域)(B)的IgG水平。
- T3(至少在第三剂 mRNA 疫苗后第 14 天)血清阳性:
- 对于总Spike IgG(包括针对刺突蛋白上可能与中和抗体无关的任何表位的活性),奥福妥单抗为62.5%(5/8)、奥利珠单抗为75.5%(9/12)、S1P为100%(7/7),健康志愿者为100%(7/7)。
- 对于更具特异性且与中和抗体相关性更好的刺突RBD IgG,奥福妥单抗为62.5%(5/8)、奥利珠单抗为50.0%(6/12)、S1P为71.4%(5/7)和健康志愿者为100% (7/7)
图 显示了每个时间点不同治疗组的T-细胞反应 – CD4+ T 细胞 (A) 和 CD8+ T 细胞 (B) 的比例具有尖峰反应性
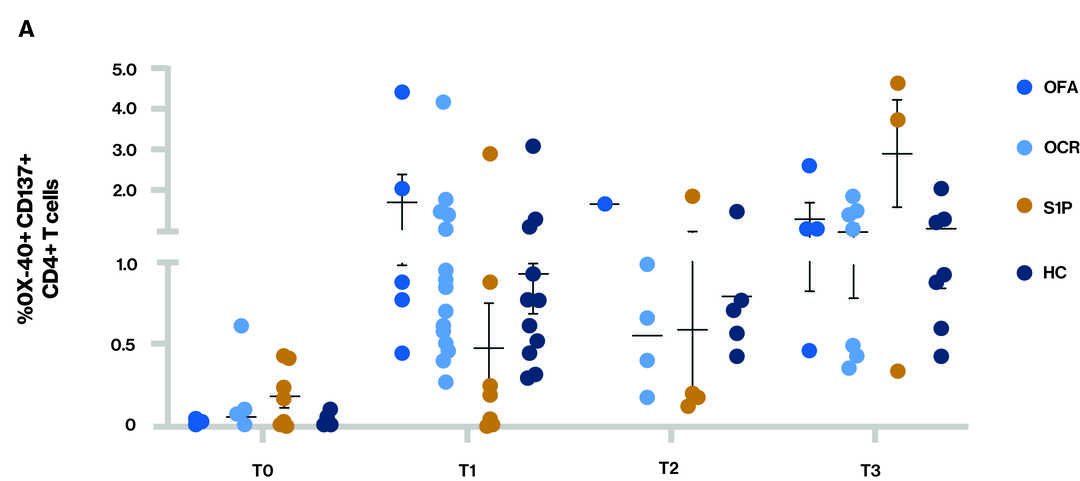
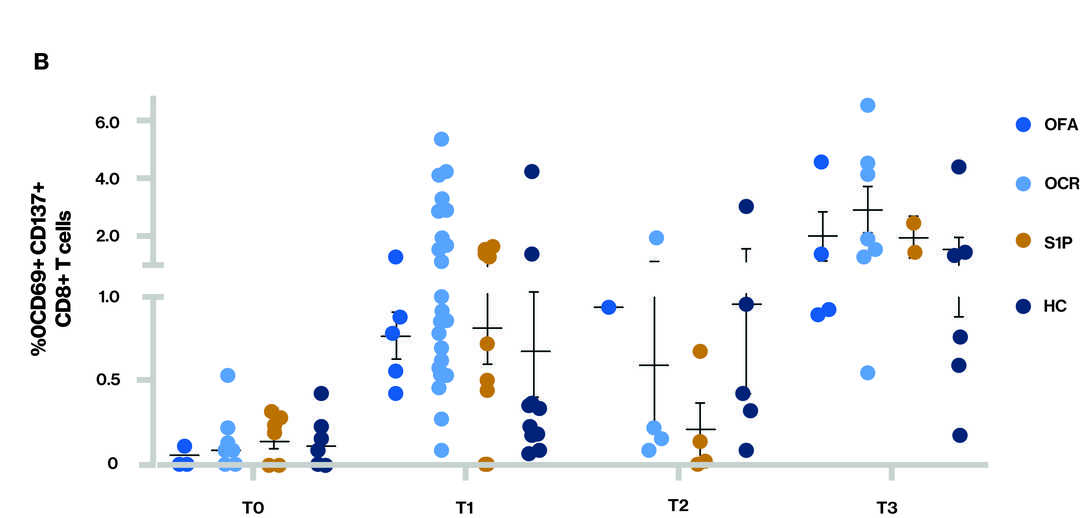
血样采集的时间点(T):T0–基线,T1–接种两剂疫苗后采集的样本,T2–接种3剂疫苗(加强针)前采集的样本和T3–接种三剂疫苗(加强针)后采集的样品;S1P(芬戈莫德和西尼莫德)
- 在T3时,所有参与者似乎都同时有CD4和CD8 T细胞反应
主要结论
- 在对S1P(芬戈利莫德和西波尼莫德)和抗CD20(奥利珠单抗和ofatumumab)治疗的成年MS患者进行的中期分析中,虽然免疫反应总体减弱,但所有DMT组的大多数患者(S1P组为 >70% 和抗CD20 为 >50%)对第三次接种(加强针)产生了抗体反应
- 在所有DMT组中,所有使用S1P和抗CD20的成年MS患者对第3剂疫苗(加强针)产生T细胞反应