TRANSFORMS
Studiendesign
Doppelblinde, randomisierte, aktiv-kontrollierte, einjährige Phase-3-Studie bei Erwachsenen mit RRMS
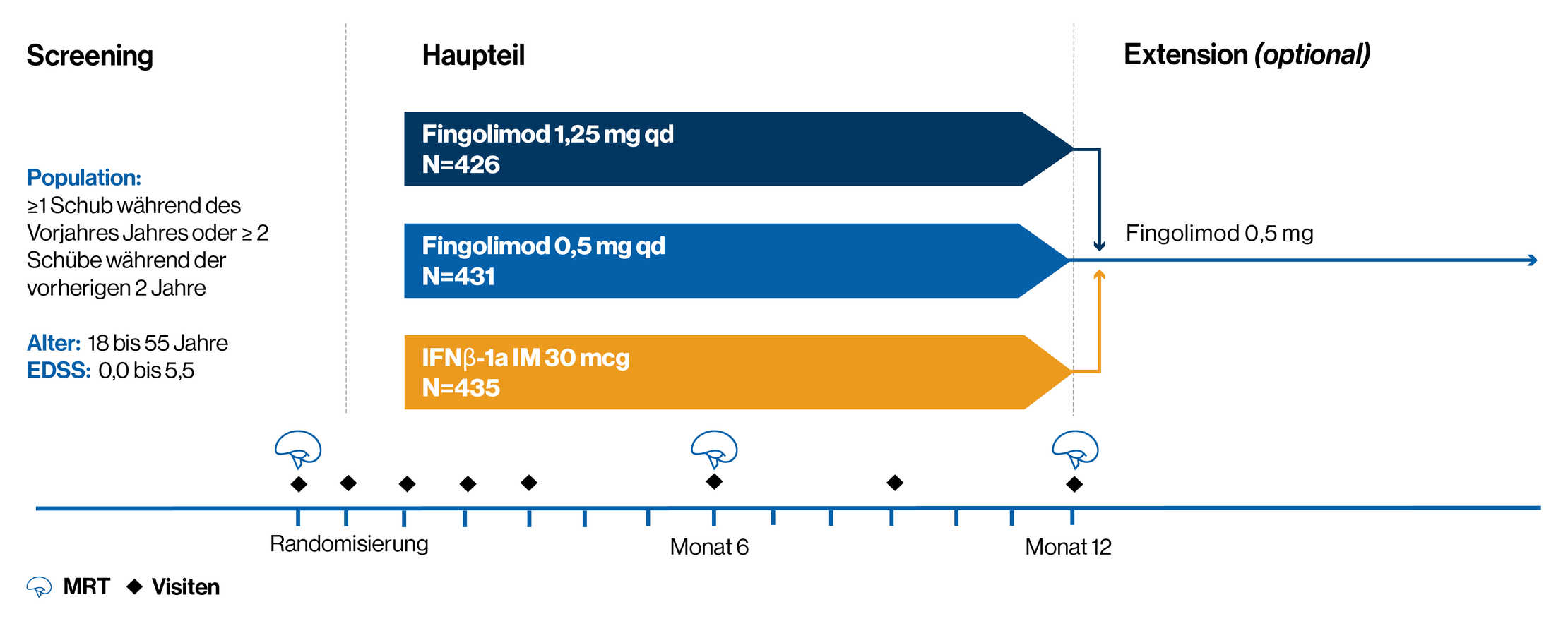
Eine 1-jährige, randomisierte, doppelblinde, aktiv-kontrollierte (IFNβ-1a IM), Phase-3-Studie mit 1.292 Erwachsenen mit RRMS
Die Patienten erhielten nach dem Zufallsprinzip eine einmal tägliche Dosis Fingolimod 0,5 mg (n = 431) oder 1,25 mg (n = 426) oder eine IFNβ-1a IM-Injektion in einer wöchentlichen Dosis von 30 μg (n = 435) für 1 Jahr.
Grundlegende Merkmale der Patienten:
1. Zwischen 18 und 55 Jahre alt
2. Eine Diagnose von RRMS mit mindestens einem dokumentierten Rückfall während des letzten Jahres oder mindestens zwei dokumentierten Rückfällen während der letzten zwei Jahre
3. Ein Score von 0,0 bis 5,5 auf dem EDSS. Der Medianwert bei Baseline betrug 2,0.
4. Previous therapy with either any type of interferon-beta or glatiramer acetate was not a criterion for exclusion
Primärer Endpunkt: Das primäre Ziel war der Nachweis, dass Fingolimod 0,5 mg bei Patienten mit RRMS, die bis zu 12 Monate lang behandelt wurden, in Bezug auf die ARR dem IFNβ-1a überlegen war.
Zwei wichtige sekundäre Endpunkte: Anzahl neuer oder neu vergrößerter hyperintenser Läsionen auf T2-gewichteten MRT-Scans nach 1 Jahr und die Zeit bis zum bestätigten Fortschreiten der Behinderung nach 3 Monaten, gemessen durch einen Anstieg des EDSS um mindestens 1 Punkt gegenüber dem Wert bei Baseline (0,5 Punkte bei Patienten mit einem Wert bei Baseline von 5,5), der über 3 Monate anhält
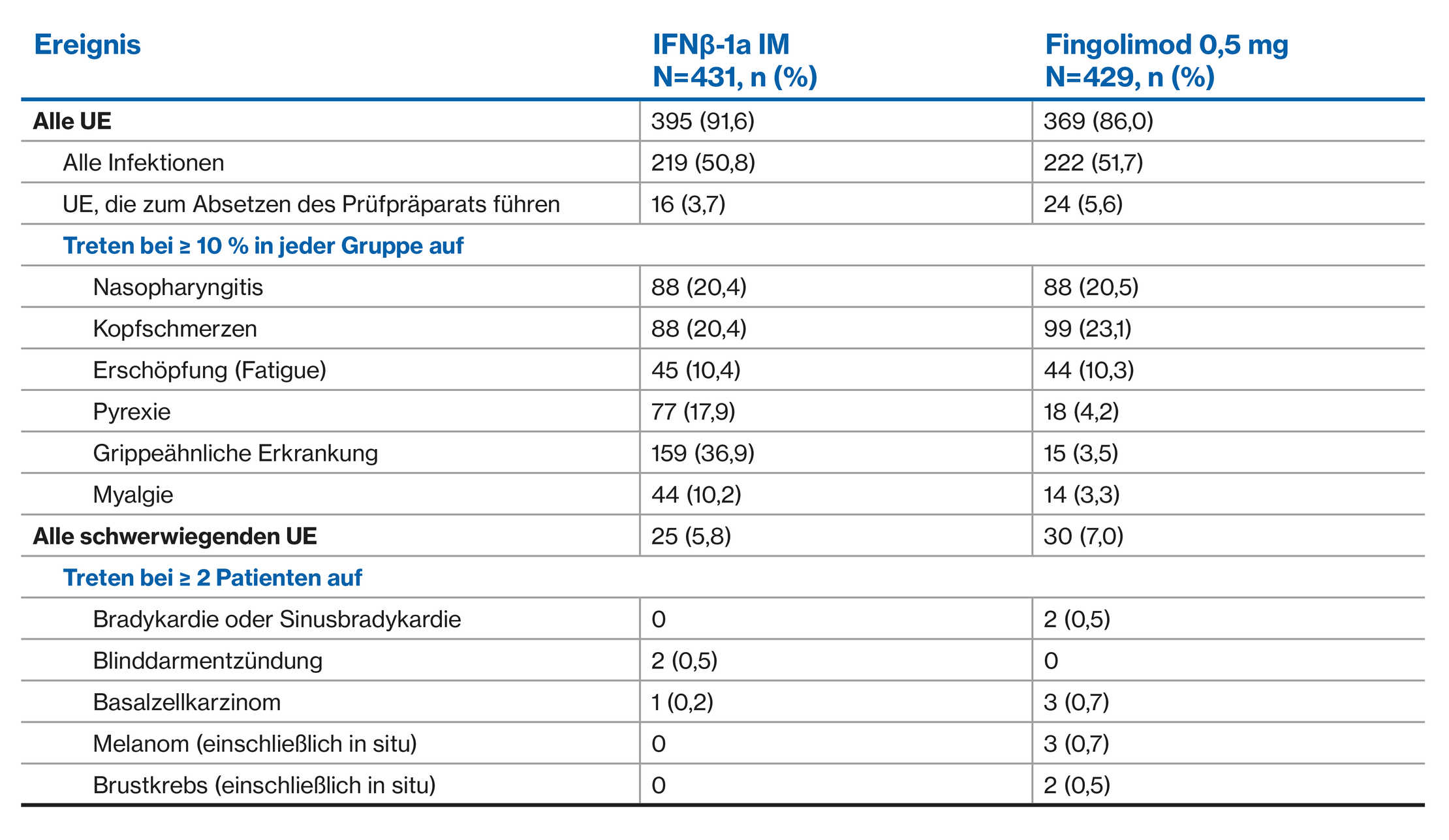
UE-Profil von Fingolimod versus Interferon über 1 Jahr: TRANSFORMS Kernstudie 1
UE-Profil von Fingolimod über 4,5 Jahre: TRANSFORMS Extensionsphase2**
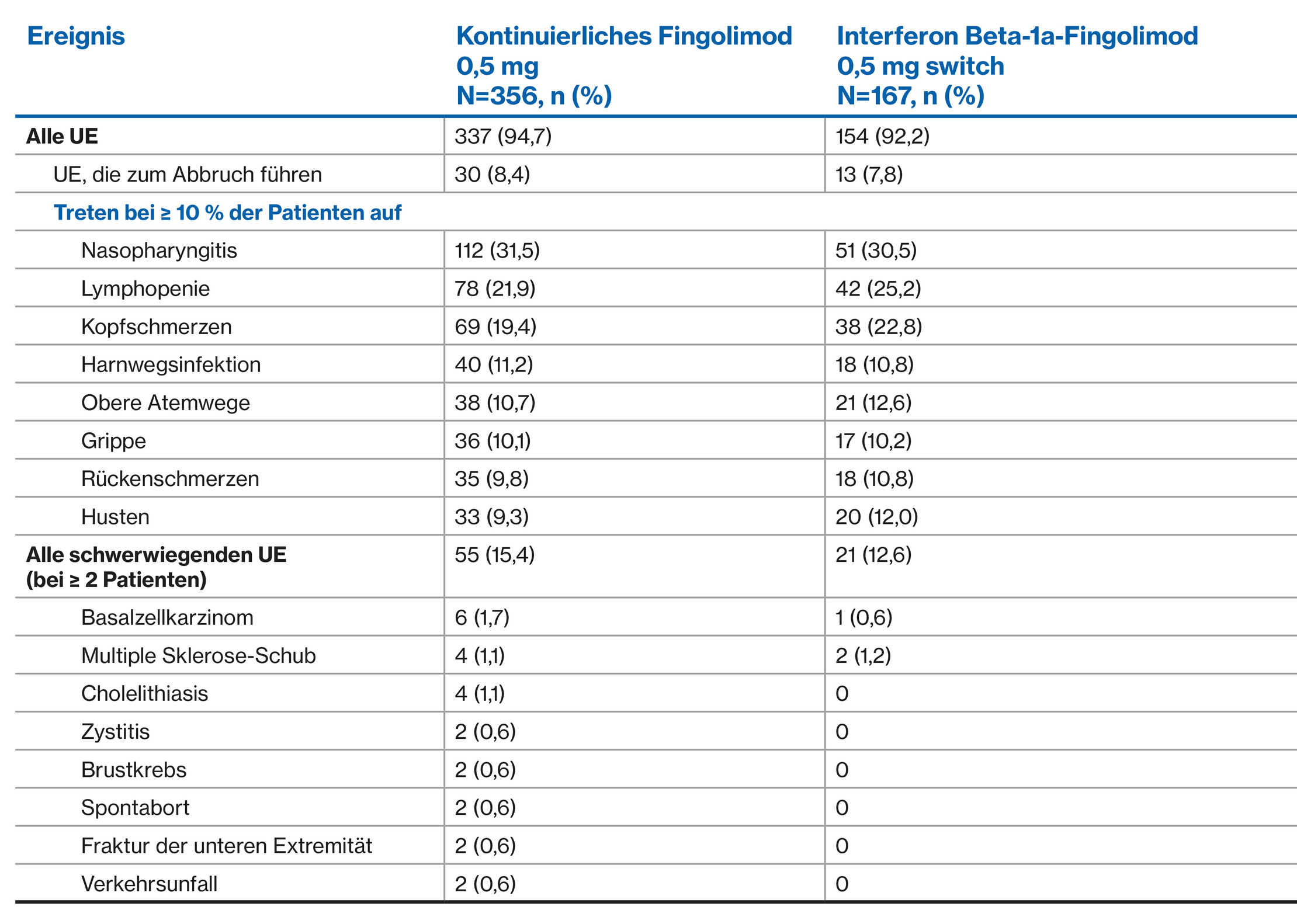
**Alle Patienten erhielten Fingolimod 0,5 mg in der Verlängerung
