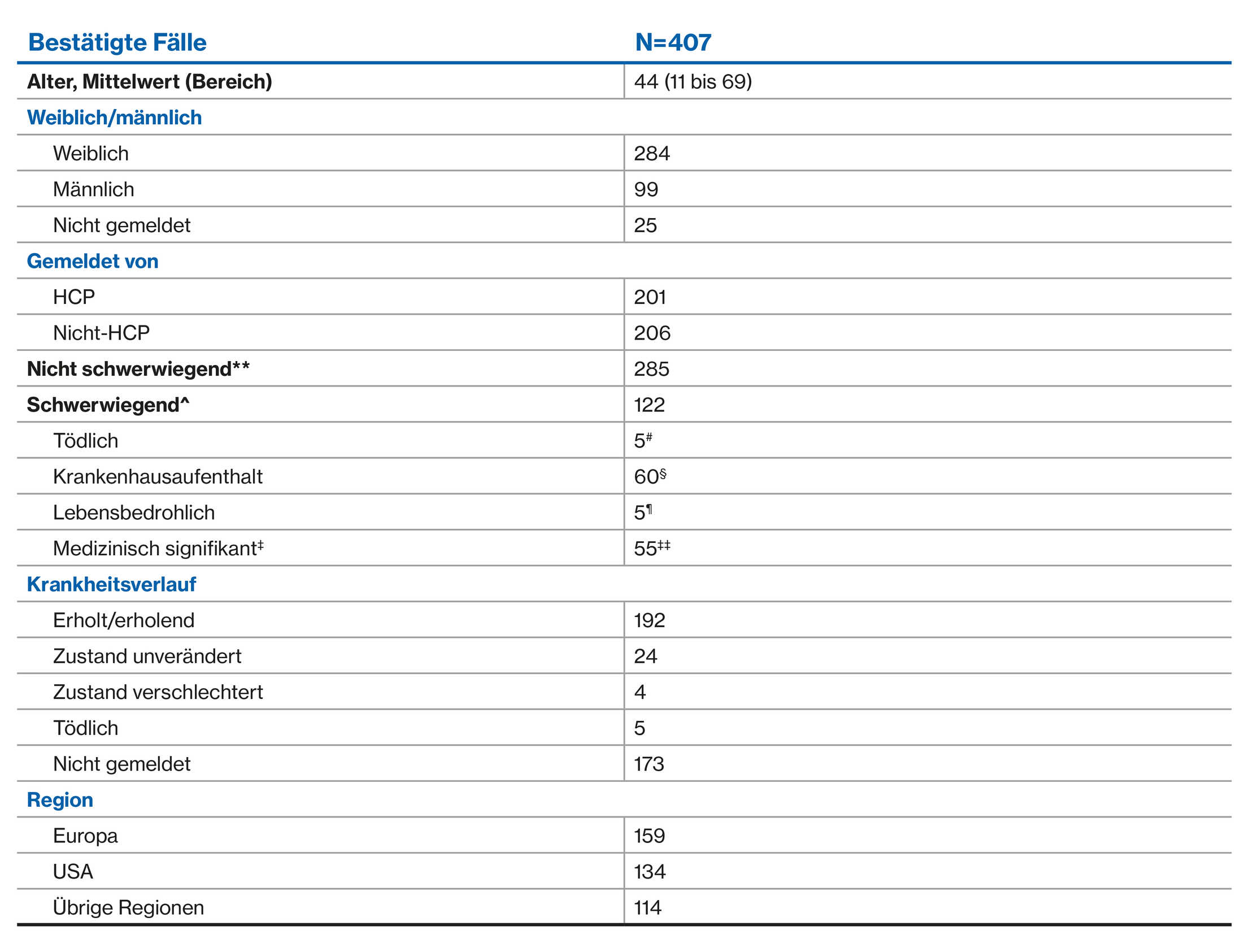
Bestätigte Fälle einer COVID-19-Infektion2
**als nicht schwerwiegend gemeldet
^Festgestellt auf der Grundlage der schwerwiegendsten Kriterien.
#Ein Patient (66 Jahre) wies mehrere Risikofaktoren auf (Einzelheiten nicht angegeben); ein Patient (39 Jahre) hatte aktive sekundär progrediente MS; ein Patient (45 Jahre) hatte eine nicht näher bezeichnete gemischte Bindegewebserkrankung; ein Patient war 64 Jahre alt und machte keine Angaben zur Krankengeschichte; ein Patient (42 Jahre) entwickelte eine disseminierte bakterielle Infektion und einen septischen Schock.
§13 von 17 Fällen (in denen Informationen gemeldet wurden) mit einem oder mehreren Risikofaktoren für COVID-19. Bei zwei Patienten mit tödlichem Ausgang wurde ebenfalls ein Krankenhausaufenthalt festgestellt, und bei einem als lebensbedrohlich gemeldeten Fall wurde ebenfalls ein Krankenhausaufenthalt festgestellt.
¶2 Fälle wurden von Nicht-HCPs gemeldet, darunter ein Patient, zu dem keine weiteren Angaben gemacht wurden, und ein weiterer Patient mit leichter Erkrankung.
‡Wichtiges medizinisches Ereignis, das zwar nicht unmittelbar lebensbedrohlich ist oder zum Tod oder Krankenhausaufenthalt führt, aber den Patienten gefährdet oder ein Eingreifen erfordert, um eine der anderen schwerwiegenden Folgen zu verhindern.
‡‡Die meisten, nämlich 39 Fälle, wurden von Nicht-HCPs eingereicht.
COVID-19 Schweregrad und Ergebnis2
HINWEIS: Der Schweregrad der Fälle wurde auf der Grundlage der COVID-19-Schweregradskala der US Food and Drug Administration3 und der Weltgesundheitsorganisation4 von einem unabhängigen Entscheidungsgremium bewertet, das sich aus Experten für MS und Infektionskrankheiten zusammensetzte; sofern Daten verfügbar waren, erfolgte die Einstufung wie folgt: asymptomatisch (Infektion ohne Symptome), leicht (kein Krankenhausaufenthalt erforderlich, Symptome umfassten keine Dyspnoe), mittelschwer (Krankenhausaufenthalt mit Lungenentzündung, die nicht als schwerwiegend gemeldet wurde und/oder mit Atemfrequenz [RR] > 20 und/oder Sauerstoffsättigung [SpO2] > 90 %, Kurzatmigkeit oder Dyspnoe, Krankenhausaufenthalt von weniger als 7 Tagen ohne weitere Angaben), schwer (Lungenentzündung, die als schwerwiegend gemeldet wurde – RR ≥ 30, SpO2 ≤ 93 %, Krankenhausaufenthalt von 7 Tagen oder mehr ohne weitere Angaben) oder kritisch (respiratorisches Versagen und/oder Intubation).
Zahlen in Klammern bedeuten – (Patienten, die ins Krankenhaus eingeliefert wurden; Patienten, die beatmet werden müssen, CPAP oder auf die Intensivstation müssen)
+Outcome is not application as these patients are asymptomatic.
ǁNicht alle mittelschweren Fälle wurden im Krankenhaus behandelt.
ǂEin Patient (66 Jahre) wies mehrere Risikofaktoren auf (Einzelheiten nicht angegeben); ein Patient (39 Jahre) hatte aktive sekundär progrediente MS; ein Patient (45 Jahre) hatte eine nicht näher bezeichnete gemischte Bindegewebserkrankung; ein Patient war 64 Jahre alt und machte keine Angaben zur Krankengeschichte; ein Patient (42 Jahre) entwickelte eine disseminierte bakterielle Infektion und einen septischen Schock.Dieser Abschnitt enthält eine Zusammenfassung der in der Novartis-Sicherheitsdatenbank gemeldeten Fälle von mit Fingolimod behandelten Patienten, bei denen entweder ein Verdacht auf COVID-19 bestand oder über die berichtet wurde, einschließlich der freiwillig eingereichten Spontanmeldungen und der in der wissenschaftlichen Literatur identifizierten Fälle. In diesem Bereich werden in der Regel zu wenige Fälle gemeldet, so dass der wahre Zähler nicht bekannt ist. Der Nenner ist ebenfalls nicht bekannt, da die tatsächliche Zahl der Patienten, die mit Fingolimod behandelt werden, nicht ohne Weiteres verfügbar ist. Viele der Fälle enthalten nur sehr begrenzte Informationen und umfassen Fälle, die nicht weiterverfolgt werden konnten. Aufgrund dieser Einschränkungen ist es daher nicht möglich, aussagekräftige Schlussfolgerungen über die Häufigkeit von COVID-19 oder den Krankheitsverlauf bei Patienten, die Fingolimod erhalten, zu ziehen.
Auswirkungen von COVID-19 bei MS in einer realen Umgebung
- MS ist eine autoimmune, chronisch-inflammatorische, neurodegenerative Erkrankung des ZNS, bei der die Patienten in der Regel mit Immunsuppressiva oder Immunmodulatoren behandelt werden.5 Die aktuelle COVID-19-Pandemie hat Bedenken hinsichtlich der Immunreaktion auf Virusinfektionen bei MS-Patienten geweckt, die mit krankheitsmodifizierenden Therapien behandelt werden.6
- Umfassender Datenaustausch und Analysen zur Wirkung von COVID-19 bei Menschen mit MS wurden von der COVID-19 in MS – GDSI durchgeführt.9 Die GDSI-Initiative ist eine gemeinsame Initiative der MS International Federation und der MS Data Alliance, die unter der Schirmherrschaft der Europäischen Charcot-Stiftung und in Zusammenarbeit mit vielen (Daten-)Partnern auf der ganzen Welt agieren.
- Bei Menschen mit MS schwankt die Häufigkeit von COVID-19 zwischen 0,5 % und 1,13 %.7 Die Sterblichkeit aufgrund von COVID-19 wurde mit 3,25 % bis 4,2 % angegeben.1,7,8
- Nach Angaben der MS Internationalen Föderation deuten die vorliegenden Erkenntnisse darauf hin, dass Menschen mit MS, die Fingolimod einnehmen, kein erhöhtes Risiko für schwerere COVID-19-Symptome haben.9